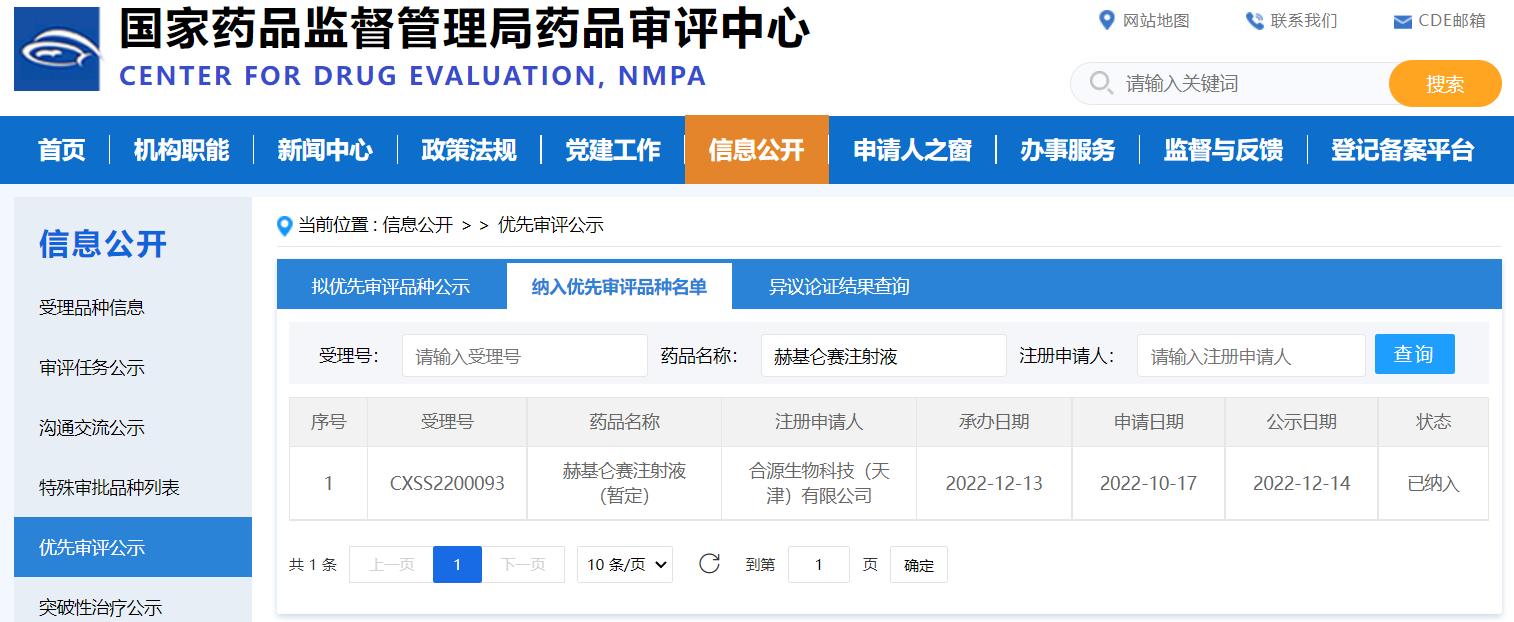
2022年12月22日,致力于成为全球领先的细胞基因前沿创新技术驱动的生物制药企业合源生物科技(天津)有限公司(以下简称“合源生物”)宣布赫基仑赛注射液(拟定)(CNCT19细胞注射液,Inaticabtagene Autoleucel)的新药上市申请(NDA)获国家药品监督管理局(NMPA)纳入优先审评审批程序,拟定适应症为:成人复发或难治性B细胞型急性淋巴细胞白血病(r/r B-ALL)。
(图片源自CDE官网)
此前,赫基仑赛注射液已获得国家药品监督管理局“突破性治疗药物(BTD)”认定和美国FDA"孤儿药"资格认定(Orphan Drug Designation, ODD)。2022年12月13日,赫基仑赛治疗成人r/r B-ALL的新药上市申请(NDA)获得国家药品监督管理局(NMPA)正式受理。
赫基仑赛注射液是首个中国全自主创新的靶向CD19的CAR-T细胞治疗产品,具有全球独特的CD19 scFv(HI19a)结构和国际领先的生产制造工艺,在成人r/r B-ALL注册临床研究中细胞药物生产成功率达到100%。赫基仑赛注射液在治疗成人r/r B-ALL的关键性临床研究中显示了持久的高缓解率和显著降低的CAR-T治疗相关毒性严重性,明显优于现有治疗手段,是治疗成人r/r B-ALL的重大突破。
优先审评审批工作程序致力于鼓励以临床价值为导向的药物创新,加快具有突出临床价值的临床急需药品上市。纳入优先审评审批工作程序将进一步加速赫基仑赛注射液的上市进程,赫基仑赛注射液有望成为中国白血病治疗领域首个上市的CAR-T产品,以满足临床急需,让患者早日获益。
https://mp.weixin.qq.com/s/AjOpnYH5UhuOYgj5tTDRNQ
关于合源生物
合源生物创立于2018年6月,是细胞与基因创新技术驱动的新一代生物医药企业,深度合作国家一流院所与临床研究中心,构建以CAR技术平台、iPSCs技术平台以及基因编辑技术平台等为核心的国际化新药研发创新体系,专注于免疫细胞治疗等创新型药物研发和商业化,致力于打造全球领先的细胞治疗药物研发、临床转化与商业化平台。
公司首个核心产品赫基仑赛注射液(拟定)(CNCT19细胞注射液,Inaticabtagene Autoleucel)是具有自主知识产权的靶向CD19的CAR-T细胞治疗产品,拥有全球独特的CD19 scFv(HI19a)结构和国际领先的生产制造工艺,先后获得国家药品监督管理局三项新药临床试验许可(IND),用于治疗成人复发或难治性急性淋巴细胞白血病、治疗复发或难治性侵袭性B细胞非霍奇金淋巴瘤和治疗儿童和青少年复发或难治B细胞型急性淋巴细胞白血病,并获得国家药品监督管理局药品审评中心“突破性治疗药物”认定和美国FDA孤儿药资格认定(Orphan Drug Designation, ODD)。国家药品监督管理局(NMPA)已正式受理赫基仑赛注射液治疗成人复发或难治性B细胞型急性淋巴细胞白血病的新药上市申请(NDA),有望成为中国白血病治疗领域首个上市的CAR-T产品和首个上市的全自主创新的靶向CD19 CAR-T产品。
公司坚持以满足临床需求为导向,通过严格的细胞治疗产品生产和质量体系,为患者打造安全、高效、可及的免疫细胞治疗产品,持续打造极具扩展性的具有国际竞争力的创新管线,覆盖血液肿瘤、实体肿瘤及自身免疫性疾病等非肿瘤疾病领域,涵盖创新型单、多靶点产品、通用型细胞治疗产品等10余种管线产品。此外,公司具有世界一流研发技术平台,工艺开发平台,质量控制体系以及商业化生产基地,并且已于2021年6月获得天津市首张细胞药物《药品生产许可证》。公司拥有多项发明专利,入选国家科技部国家重点研发计划项目即“科技助力经济2020重点专项项目”。

 查看更多 +
查看更多 +
 010-65960020
010-65960020
 pr@juventas.cn
pr@juventas.cn

